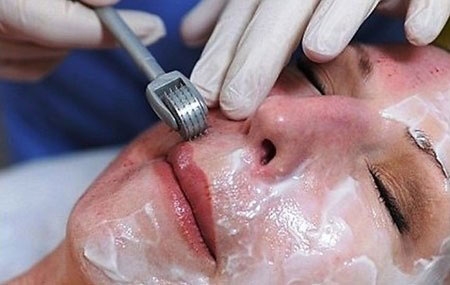
Dùng mỹ phẩm làm từ nhau thai - Rước mầm bệnh vào người
Dữ liệu cũ 30/03/2015, 11:14Mới đây, Cục Quản lý dược - Bộ Y tế đã phải ban hành công văn về việc không cấp phép cho bất kỳ mỹ phẩm nào có chứa nhau thai và tế bào gốc có nguồn gốc từ con người. Cục Quản lý dược phải ra lệnh này là vì tình trạng kinh doanh, quảng cáo các loại mỹ phẩm có chứa nhau thai đang rất rầm rộ khiến nhiều chị em ngộ nhận về tác dụng kỳ diệu của nó mà không hay biết đó là mầm bệnh nguy hiểm.

Mỹ phẩm “handmade” bị “sờ gáy”
Dữ liệu cũ 25/03/2015, 10:44Trước tình trạng mỹ phẩm tự làm (handmade) được rao bán tràn lan trên mạng, không được kiểm định về chất lượng, nguy cơ ảnh hưởng đến sức khỏe người sử dụng, Cục Quản lý Dược (Bộ Y tế) cho biết sẽ siết chặt quản lý mỹ phẩm tự chế.
Đình chỉ hai loại thuốc chữa dạ dày, tá tràng
Dữ liệu cũ 03/02/2015, 14:05Mẫu kiểm nghiệm hai loại thuốc Pantopep-Dol (Pantoprazol 40mg) và thuốc Pantocid (Pantoprazole tablets 40mg cho thấy không đạt chỉ tiêu chất lượng nên đã bị đình chỉ lưu hành trên toàn quốc.
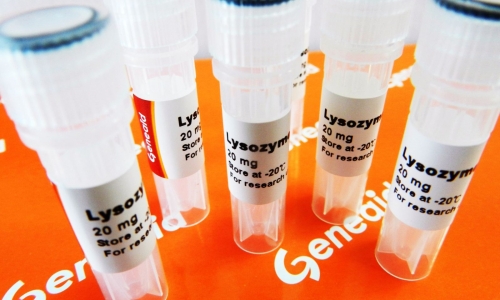
Đình chỉ và thu hồi 38 thuốc có hoạt chất Lysozym
Dữ liệu cũ 31/01/2015, 10:07Ngày 30/1, ông Đỗ Văn Đông, Cục phó Cục Quản lý Dược (Bộ Y tế), cho biết vừa có văn bản gửi Sở Y tế các tỉnh, TP; các đơn vị sản xuất, kinh doanh, xuất nhập khẩu thuốc; các BV, viện có giường bệnh yêu cầu đình chỉ và thu hồi các loại thuốc chứa hoạt chất Lysozym.

Thuốc Prednisolon 5mg của Công ty dược OPV bị làm giả
Dữ liệu cũ 07/01/2015, 15:13Cục Quản lý dược cũng yêu cầu Sở Y tế tỉnh Trà Vinh phối hợp với các cơ quan chức năng để truy tìm nguồn gốc xuất xứ của lô thuốc Prednisolon 5mg giả

Triclosan trong kem đánh răng: vẫn gây tranh luận
Dữ liệu cũ 19/08/2014, 08:44Ngày 18/8, Cục quản lý dược (Bộ Y tế) cho biết, sau khi có thông tin kem đánh răng Colgate có chất Triclosan (được Cục quản lý thực phẩm và dược phẩm Hoa Kỳ cho là có thể gây ung thư), cục đã xác minh thông tin với Hiệp định mỹ phẩm ASEAN.

Nhiều bệnh nhân ngộ độc nấm đã tử vong
Dữ liệu cũ 24/03/2014, 18:50Nhiều bệnh nhân bị ngộ độc nấm trong thời gian qua đã tử vong. Cục quản lý Dược (Bộ Y tế) đã chỉ đạo các đơn vị đảm bảo đủ thuốc cho nhu cầu điều trị ngộ độc.

Cảnh báo phản ứng phụ của thuốc chứa paracetamol
Dữ liệu cũ 20/02/2014, 18:00Cục Quản lý dược (Bộ Y tế) vừa gửi văn bản yêu cầu các công ty đăng ký, sản xuất thuốc chứa hoạt chất paracetamol phải cập nhật, cảnh báo nguy cơ phản ứng phụ nghiêm trọng trên da.
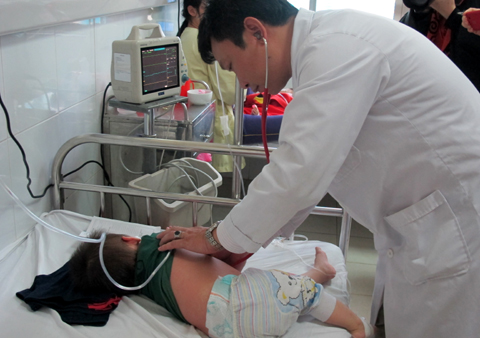
Khẩn cấp nhập gần 80.000 liều vắc xin thủy đậu
Dữ liệu cũ 20/02/2014, 11:05– Cục Quản lý Dược (Bộ Y tế) đề nghị các Sở Y tế và đơn vị sản xuất, kinh doanh, nhập khẩu và đăng ký lưu hành vắc xin cần đảm bảo cung ứng vắc xin cho công tác phòng bệnh thủy đậu.

Đình chỉ lưu hành thuốc viên nén bao phim Roxl-150
Dữ liệu cũ 09/01/2014, 10:05Ngày 28/11/2013, Cục Quản lý Dược (Bộ Y tế) có công văn thông báo quyết định đình chỉ lưu hành thuốc không đạt tiêu chuẩn chất lượng đối với thuốc viên nén bao phim Roxl-150 (Roxithromycin 150mg), Số lô: B868, HD: 05/06/15, SĐK: VN-13935-11, do Công ty XL Laboratories Pvt. Ltd – India sản xuất, Công ty TNHH 1 TV Dược phẩm Trung ương 2 nhập khẩu. Trong thông báo gửi Sở Y tế các tỉnh, thành phố trực thuộc Trung ương và Công ty TNHH 1 thành viên Dược phẩm Trung ương 2, Cục Quản lý Dược (Bộ Y tế) cho biết căn cứ các quy định về quản lý dược hiện hành của Việt Nam và căn cứ công văn số 361/VKNT-KHTH ngày 11/11/2013 của Viện Kiểm nghiệm thuốc Tp. Hồ Chí Minh gửi kèm phiếu kiểm nghiệm 0489/VKN-KT2013 ngày 11/11/2013 về thuốc viên nén bao phim Roxl-150 (Roxithromycin 150mg), Số lô: B868, HD: 05/06/15, SĐK: VN-13935-11, do Công ty XL Laboratories Pvt. Ltd – India sản xuất, Công ty TNHH 1 TV Dược phẩm Trung ương 2 nhập khẩu.

Đình chỉ lưu hành thuốc Fenactada
Dữ liệu cũ 08/01/2014, 14:50Ngày 10/12/2013, Cục Quản lý Dược (Bộ Y tế) ban hành quyết định đình chỉ lưu hành thuốc không đạt tiêu chuẩn chất lượng đối với thuốc Fenactada và các đơn vị phải báo cáo kết quả thu hồi thuốc này về Cục Quản lý Dược trước 6/1/2014. Trong công văn gửi Sở Y tế các tỉnh, thành phố trực thuộc Trung ương và công ty Cổ phần dược Lâm Đồng, Cục Quản lý Dược cho biết căn cứ các quy định về quản lý dược hiện hành của Việt Nam và căn cứ công văn số 1142/VKNTTW-KH ngày 25/11/2013 của Viện Kiểm nghiệm thuốc Trung ương gửi kèm Phiếu kiểm nghiệm số 43Gt70 ngày 25/11/2013 về thuốc viên nén bao phim Fenactada (Diclofenac natri 75mg), Số lô: 010412, NSX: 02/05/2012, HD: 02/05/2015, SĐK: VD-15089-11 do Công ty Cổ phần dược Lâm Đồng sản xuất.

Đình chỉ lưu hành thuốc Penfixil 100
Dữ liệu cũ 08/01/2014, 10:50Ngày 26/11/2013, Cục Quản lý Dược (Bộ Y tế) có văn bản thông báo số:19687/QLD-CL về việc đình chỉ lưu hành thuốc không đạt tiêu chuẩn chất lượng đối với thuốc Penfixil 100. Trong công văn gửi Sở Y tế các tỉnh, thành phố trực thuộc Trung ương và Công ty Cổ phần Dược VTYT Đắk Lắk, Cục Quản lý Dược cho biết căn cứ các quy định về quản lý dược hiện hành của Việt Nam và căn cứ công văn số 1039/VKNTTW-KH ngày 05/11/2013 của Viện Kiểm nghiệm thuốc Trung ương gửi kèm Phiếu kiểm nghiệm số 43Gt62 ngày 04/11/2013 về thuốc Bột pha hỗn dịch uống Penfixil 100 (Cefpodoxime 100mg), Số lô: 139313002, NSX: 08/01/2013, HD: 07/01/2015, SĐK: VN-11393-10, do Công ty Penta Labs Pvt. Ltd., India sản xuất, Công ty Cổ phần Dược VTYT Đắk Lắk nhập khẩu.

66 cơ sở SX thuốc nước ngoài vi phạm chất lượng
Vấn đề liên quan 07/01/2014, 16:50Ngày 3/11/2013, Cục Quản lý Dược có thông báo về danh sách các cơ sở sản xuất thuốc nước ngoài có thuốc vi phạm chất lượng phải lấy mẫu kiểm tra chất lượng 100% lô (từ ngày 01/01/2011 đến ngày 25/10/2013). Theo đó, có 66 cơ sở sản xuất thuốc nước ngoài có thuốc vi phạm chất lượng phải lấy mẫu kiểm tra chất lượng 100% lô. 66 công ty này thuộc 12 quốc gia, trong đó Ấn Độ là nước có nhiều công ty có thuốc vi phạm chất lượng nhất (với tổng số 45 công ty).

Hiệu thuốc đổi chủ phải xin cấp lại chứng nhận GPP
Dữ liệu cũ 07/01/2014, 16:50Việc thẩm định các hoạt động cơ sở bán lẻ thuốc đạt GPP đều liên quan đến người quản lý chuyên môn hoặc chủ cơ sở. Vì vậy khi thay đổi người quản lý chuyên môn hoặc chủ cơ sở phải kiểm tra và cấp giấy GPP của cơ sở bán lẻ thuốc như cơ sở mới. Cục Quản lý Dược cho biết nhận được Công văn số 7307/SYT-QLDVYT đề ngày 04/11/2013 của Sở Y tế thành phố Hồ Chí Minh về việc cấp lại giấy chứng nhận GPP và GDP;

Rà soát thuốc có hàm lượng, công thức lạ
Dữ liệu cũ 07/01/2014, 16:50Toàn bộ những thuốc có hàm lượng bất thường, công thức lạ sẽ được rà soát lại và yêu cầu nhà sản xuất giải trình. Cục Quản lý Dược, Bộ Y tế cho biết, Hội đồng xét cấp đăng ký thuốc sẽ rà soát lại các thuốc có hàm lượng bất thường, công thức lạ đã được cấp số đăng ký.
